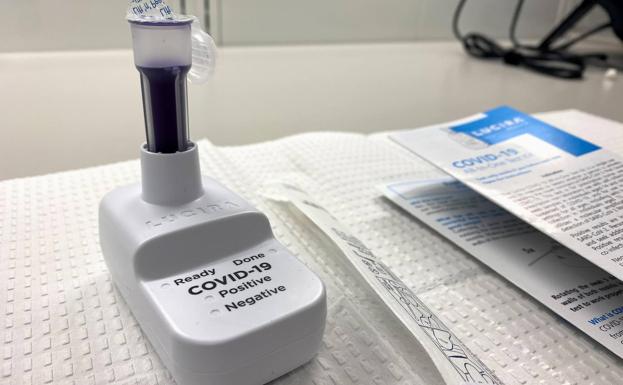
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) ha emitido la autorización de uso de emergencia (EUA, por sus siglas en inglés) para la primera prueba de autodiagnóstico de COVID19 en casa y que proporciona resultados en unos 30 minutos. El kit, ha sido creado por la compañía Lucira y consiste en una prueba monocular de un solo uso que funciona de forma sencilla.
En concreto, la persona se toma la muestra como hisopo nasal y la lectura del resultado es un LED luminoso en el dispositivo de lectura, que indica positivo o negativo en COVID19. Dicha prueba se llama “Lucira COVID19 All-In-One Test Kit” y ha sido autorizada para su uso en el hogar con muestras de hiposado nasal en personas de 14 años o más que son sospechosas de padecer la enfermedad.
Está autorizada para el uso en consultorios médicos, Urgencias y hospitales
Asimismo, esta prueba está autorizada para el uso en hospitales, consultorios médicos, centros de atención urgente y Urgencias para todas las edades, pero las muestras deben ser recogidas por un médico cuando la prueba se utiliza para examinar a los individuos menores de 14 años. En la actualidad, la prueba está autorizada exclusivamente para su uso con receta médica.
Esta prueba funciona haciendo girar el hisopo de la muestra recogida en un vial que luego se coloca en la unidad de prueba. En 30 minutos, aproximadamente, los resultados pueden leerse directamente en la pantalla luminosa de la unidad de prueba que muestra si una persona es positiva o negativa para el virus SARS-CoV-2.
Lucira Health es el fabricante de la prueba de autodiagnóstico
Los médicos que prescriben la prueba están obligados a comunicar todos los resultados de las pruebas que reciben de las personas que las utilizan a sus autoridades de salud pública competentes, según con los requisitos locales, estatales y federales.
El fabricante de la prueba, Lucira Health también ha elaborado un etiquetado de la caja, instrucciones de referencia rápida e instrucciones para los proveedores de atención de la salud para ayudar a la presentación de informes.
Este test ha logrado un 94% de acuerdo porcentual positivo (PPA) y un 98 por ciento de acuerdo porcentual negativo (MPA). Excluyendo las muestras con niveles muy bajos de virus que, posiblemente ya no reflejaban una infección activa1, Lucira logró un acuerdo porcentual positivo del 100 por cien.